Upotreba alkana
Korištenje alkana je vrlo raznolik - oni se koriste kao gorivo, kao i za mehaniku, medicinu itd. Uloga tih kemijskih spojeva u životu suvremenog čovjeka teško je precijeniti.
sadržaj
Alkani: svojstva i kratke značajke
Alkanes su ne-ciklički ugljikovi spojevi u kojima su atomi ugljika vezani jednostavnim zasićenim vezama. Te tvari su serija s određenim svojstvima i svojstvima. Opća formula alkana je sljedeća:
CnH2n + 2
Ovdje je broj ugljikovih atoma. Na primjer, CH3, C2H6.
Prva četiri predstavnika brojnih alkana - plinovitih tvari - su metan, etan, propan i butan. Sljedeći spojevi (C5 do C17) su tekućine. Serija se nastavlja spojevima koji su pod normalnim uvjetima krute tvari.
Što se tiče kemijskih svojstava, alkani su neaktivni - oni praktički ne djeluju u interakciji s alkalijama i kiselinama. Usput, to su kemijska svojstva koja određuju uporabu alkana.
Ipak, određene reakcije su karakteristične za te spojeve, uključujući supstituciju atoma vodika, kao i postupke razdvajanja molekula.
- Najkarakterističnija reakcija je halogeniranje u kojem su atomi vodika zamijenjeni halogenom. Vrlo su važne reakcije kloriranja i bromiranja ovih spojeva.
- Nitriranje je zamjena vodikovog atoma nitro skupinom u reakciji s razrijeđenom (10% -tnom koncentracijom) dušična kiselina. U normalnim uvjetima, alkani ne djeluju međusobno s kiselinama. Da bi se provela slična reakcija, potrebna je temperatura od 140 ° C.
- Oksidacija - u normalnim uvjetima, alkani ne reagiraju na kisik. Ipak, nakon puštanja u zrak, ove tvari ulaze u reakcija izgaranja, konačni proizvodi od kojih su voda i ugljični dioksid.
- Pukotina - ova reakcija odvija se samo kada postoje potrebni katalizatori. U tom procesu se odcjepljuju stabilne homološke veze između ugljikovih atoma. Na primjer, s puferom butana, reakcija može proizvesti etan i etilen.
- Izomerizacija - kao posljedica djelovanja određenih katalizatora, moguće je određene promjene alkana ugljikovog kostura.
Upotreba alkana
Glavni prirodni izvor tih tvari su vrijedni proizvodi poput prirodnog plina i ulja. Područja primjene alkana danas su vrlo široka i raznolika.
Na primjer, plinovite tvari koristiti kao vrijedan izvor goriva. Primjer je metan, od kojeg se sastavlja prirodni plin, kao i smjesa propana-butana.
Još jedan izvor alkana - ulje, što je teško nadvladati za suvremeno čovječanstvo. Proizvodi nafte uključuju:
- benzin - koristi se kao gorivo;
- kerozin;
- dizelskog goriva ili lakog plinskog ulja;
- Masno plinsko ulje, koje se koristi kao ulje za podmazivanje;
- stanja destilacija nafte koristi se za proizvodnju asfalta.
Naftni proizvodi se također koriste za proizvodnju plastike, sintetičkih vlakana, guma i nekih deterdženata.
Ali upotreba alkana je mnogo širi. Neki tekući oblici ovih tvari koriste se kao otapala, kao i kao raketno gorivo.
Vazelin i vazelina su proizvodi koji se sastoje od mješavine alkana. Oni se koriste u medicini i kozmetika (uglavnom za pripremu masti i kreme), kao i parfeme.
Parafin je drugi dobro poznati proizvod koji je mješavina krutih alkana. To je čvrsta bijela masa, čija temperatura zagrijavanja iznosi 50 - 70 stupnjeva. U modernoj proizvodnji parafina se koristi za izradu svijeća. Ista tvar je impregnirana sa šibicama. U medicini se, uz pomoć parafina, provode različite termičke procedure.
 Fizička svojstva aldehida
Fizička svojstva aldehida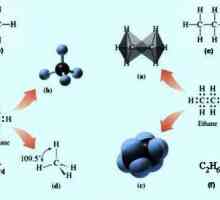 Kako dobiti alkan iz alkana? Što još možete dobiti od alkana?
Kako dobiti alkan iz alkana? Što još možete dobiti od alkana? Postupci za proizvodnju alkena: laboratorij i industrijski
Postupci za proizvodnju alkena: laboratorij i industrijski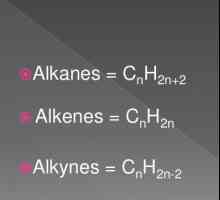 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena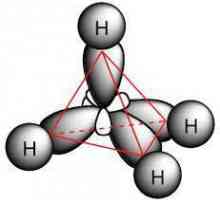 Koji alkani su karakterizirani reakcijama
Koji alkani su karakterizirani reakcijama Kemijska svojstva alkina. Struktura, prijem, primjena
Kemijska svojstva alkina. Struktura, prijem, primjena Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Kako napraviti izomere i homologe? Kako napraviti izomere alkana? Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane Kako odrediti kvalitativni i kvantitativni sastav tvari
Kako odrediti kvalitativni i kvantitativni sastav tvari Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva
Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva Što je sustavna nomenklatura
Što je sustavna nomenklatura Što su alifatski ugljikovodici?
Što su alifatski ugljikovodici? Pentan: izomeri i nomenklatura
Pentan: izomeri i nomenklatura Kemijska svojstva alkana
Kemijska svojstva alkana Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva
Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva Serije homologije
Serije homologije Alkanes: kemijska svojstva
Alkanes: kemijska svojstva Kemijska svojstva alkena (olefina)
Kemijska svojstva alkena (olefina) Izomeri heptana: opća karakteristika i primjena
Izomeri heptana: opća karakteristika i primjena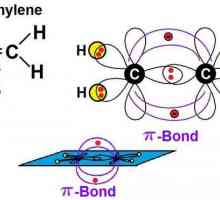 Alkeni: formula. Kemijska svojstva. recepcija
Alkeni: formula. Kemijska svojstva. recepcija Propan je ekološko gorivo. Njegova fizička i kemijska svojstva
Propan je ekološko gorivo. Njegova fizička i kemijska svojstva
 Kako dobiti alkan iz alkana? Što još možete dobiti od alkana?
Kako dobiti alkan iz alkana? Što još možete dobiti od alkana? Postupci za proizvodnju alkena: laboratorij i industrijski
Postupci za proizvodnju alkena: laboratorij i industrijski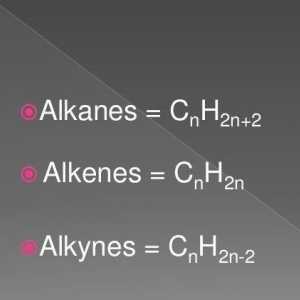 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena Koji alkani su karakterizirani reakcijama
Koji alkani su karakterizirani reakcijama Kemijska svojstva alkina. Struktura, prijem, primjena
Kemijska svojstva alkina. Struktura, prijem, primjena Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Kako napraviti izomere i homologe? Kako napraviti izomere alkana? Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane Kako odrediti kvalitativni i kvantitativni sastav tvari
Kako odrediti kvalitativni i kvantitativni sastav tvari Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva
Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva Što je sustavna nomenklatura
Što je sustavna nomenklatura