Kemijska svojstva alkana
Metana i njegovi homolozi naziva granica (zasićen) parafinski ugljikovodici ili alkani. Posljednjih navedenih organskih tvari (imaju opću kemijska formula CnH2n + 2, koji odražava zasićenje molekula, atoma koji su povezani kovalentnim vezama jednostavnim ugljik-vodik ili ugljik-ugljik) je dodijeljen u skladu s Međunarodnom nomenklature kemijskih spojeva. Imaju dva glavna izvora: sirove nafte i prirodni plin. Svojstva alkana u serija homologije
sadržaj
Prva četiri predstavnika homologne serije povijesno su formirala imena. Ugljikovodici iza njih označeni su grčkim brojevima s završetkom -an. Relativna molekularna težina Svaki slijedeći ugljikovodik razlikuje se od prethodne sa 14 amu. Fizička svojstva alkani kao što je talište (točka vrenja) i točka vrenja (kondenzacija), gustoća i indeks refrakcije rastu uz povećanje molekulske mase. Od metana do butana su plinovi, od pentana do pentadekan-tekućine, a zatim slijedite krute tvari. Svi parafini su lakši od vode i ne rastopiti se u njoj. Alkani uključuju:
- CH4 je metan;
- C2H6 - etan;
- C3H8 - propan;
- C4Hio je butan;
- C5H12 - pentan;
- C6H14 - heksan;
- C7H16 - heptan;
- C8H18 - oktan;
- C9H20 - nonan;
- C10H22-dekan;
- C11H24 - undekana;
- C12H26 - dodekan;
- C13H28 - tridekan;
- C14H30 - tetradekan;
- C15H32 - pentadecane;
- C16H34 - heksadekan;
- C17H36 - heptadekan;
- C18H38 - okadekan;
- C19H40 - nonadecan;
- C20H42-eikozan i tako dalje.
Kemijska svojstva alkana karakterizira niska aktivnost. To se objašnjava relativnom čvrstoćom nepolarnih C-C i niskopolarnih C-H veza, kao i zasićenosti molekula. Svi atomi su povezani singlom sigma - veze koje je teško uništiti zbog svoje niske polarizabilnosti. Njihovo se pukotina može ostvariti samo pod određenim uvjetima, uz formiranje radikala koji nose imena odgovarajućih parafinskog spoja zamjenom završetka. Na primjer, propan-propil (C3H7-), etan-etil (C2H5-), metan-metil (CH3-) i tako dalje.
Kemijska svojstva alkana pokazuju inertnost ovih spojeva. Nisu sposobni pridružiti se reakcijama. Reakcije su tipične za njih. Oksidacija (sagorijevanjem) javlja se samo parafinski ugljikovodici, na povišenoj temperaturi. Mogu se oksidirati u aldehide i alkohola, kiseline. Kao jedan rezultat kreginga (postupak toplinske cijepanja ugljikovodika) viši alkana pri temperaturi od 450 do 550 ° C, može tvoriti zasićeni ugljikovodik s nižom molekularnom težinom. Uz povećanje temperature, termička razgradnja se naziva pirolizom.
Kemijska svojstva alkana ne ovisi samo o broju atoma ugljika u molekuli, kao i na strukturu. Sve uobičajene parafini se može odvojiti (jedan atom ugljika može biti povezan s ne više od dva atoma ugljika) i izo-struktura (C atom može biti povezan na četiri atoma C kroz ove molekule ima prostornu strukturu). Na primjer pentan, 2,2-dimetilpropana imaju istu molekularnu težinu i kemijske formule C5H12, ali je kemijska i fizikalna svojstva su razlikuju: talište 129.7 ° C, minus i minus 16,6 ° C, 36,1 ° C vrenja i 9,5 ° C, respektivno. Izomeri mogu lako ući kemijske reakcije, od ugljikovodika normalne strukture s istim brojem C atoma.
Karakteristična kemijska svojstva alkana su supstitucijske reakcije, koji uključuju halogeniranje ili sulfoniranje. Reakcija klora s parafina diradikalom mehanizma pod utjecajem topline ili svjetla generira klorirani metan: klormetan CH3Cl, diklormetan CH2Cl2, CHCl3 triklormetan i ugljik-tetraklorid CCl4. Kada je pod UV svjetlom, kloridi sulfonske kiseline dobije se sulfoniranje alkani: R = H + SO2 + Cl2 → R-SO2-Cl + HCl. Te tvari se koriste u proizvodnji površinski aktivnih tvari.
 Formula benzena: koja od varijacija je točna?
Formula benzena: koja od varijacija je točna? Fizička svojstva aldehida
Fizička svojstva aldehida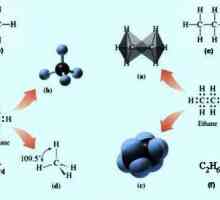 Kako dobiti alkan iz alkana? Što još možete dobiti od alkana?
Kako dobiti alkan iz alkana? Što još možete dobiti od alkana?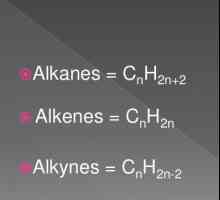 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena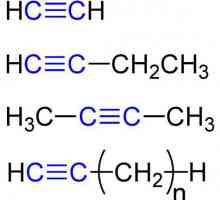 Kemijska svojstva alkina. Struktura, prijem, primjena
Kemijska svojstva alkina. Struktura, prijem, primjena Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Kako napraviti izomere i homologe? Kako napraviti izomere alkana? Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane Alkadieni su tipični predstavnici nezasićenih ugljikovodika
Alkadieni su tipični predstavnici nezasićenih ugljikovodika Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena
Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena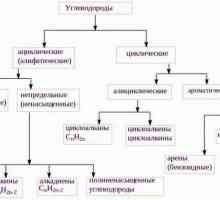 Što su alifatski ugljikovodici?
Što su alifatski ugljikovodici?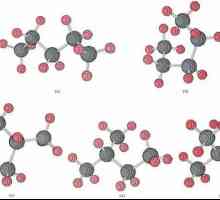 Pentan: izomeri i nomenklatura
Pentan: izomeri i nomenklatura Zasićeni ugljikovodici: svojstva, formule, primjeri
Zasićeni ugljikovodici: svojstva, formule, primjeri Izgaranje metana
Izgaranje metana Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva
Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva Serije homologije
Serije homologije Upotreba alkana
Upotreba alkana Alkanes: kemijska svojstva
Alkanes: kemijska svojstva Kemijska svojstva alkena (olefina)
Kemijska svojstva alkena (olefina) Izomeri heptana: opća karakteristika i primjena
Izomeri heptana: opća karakteristika i primjena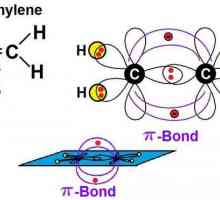 Alkeni: formula. Kemijska svojstva. recepcija
Alkeni: formula. Kemijska svojstva. recepcija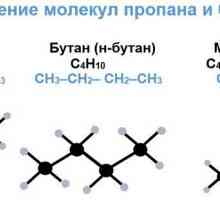 Propan je ekološko gorivo. Njegova fizička i kemijska svojstva
Propan je ekološko gorivo. Njegova fizička i kemijska svojstva
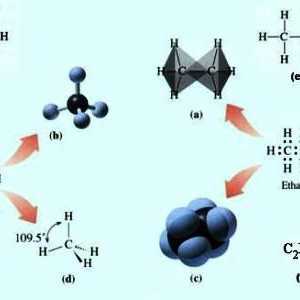 Kako dobiti alkan iz alkana? Što još možete dobiti od alkana?
Kako dobiti alkan iz alkana? Što još možete dobiti od alkana?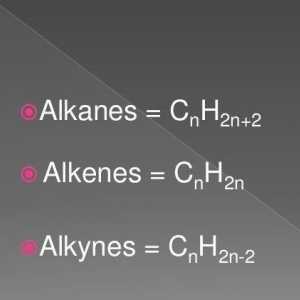 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena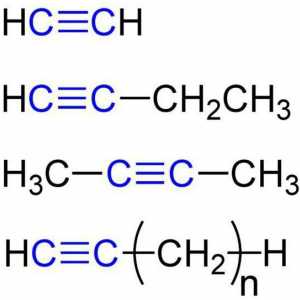 Kemijska svojstva alkina. Struktura, prijem, primjena
Kemijska svojstva alkina. Struktura, prijem, primjena Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Kako napraviti izomere i homologe? Kako napraviti izomere alkana? Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane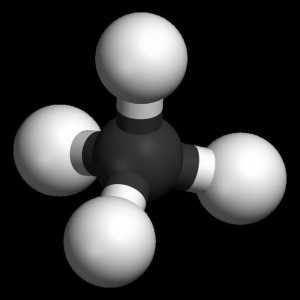 Alkadieni su tipični predstavnici nezasićenih ugljikovodika
Alkadieni su tipični predstavnici nezasićenih ugljikovodika Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena
Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena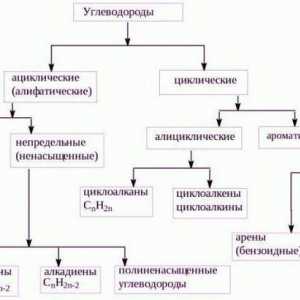 Što su alifatski ugljikovodici?
Što su alifatski ugljikovodici? Pentan: izomeri i nomenklatura
Pentan: izomeri i nomenklatura