Makromolekula je molekula s visokom molekularnom masom. Konfiguracija makromolekule
Makromolekula je molekula koja ima veliku molekularnu težinu. Njegova struktura je zastupljena u obliku ponavljajućih veza. Razmotrimo značajke takvih spojeva, njihov značaj za vitalnu aktivnost živih bića.
sadržaj

Značajke sastava
Biološke makromolekule formiraju se iz stotina tisuća malih početnih tvari. Za žive organizme postoje tri glavne vrste makromolekula: proteini, polisaharidi, nukleinske kiseline.
Monosaharidi, nukleotidi, aminokiseline služe kao početni monomeri za njih. Makromolekula je gotovo 90 posto mase stanica. Ovisno o slijedu aminokiselinskih ostataka, nastaje specifična molekula proteina.
Visoke molekularne tvari su one koje imaju molarnu masu veću od 103 Da.

Povijest izgleda
Kada se pojavila makromolekula? Ovaj je koncept uveden Nobelovim laureatom u području kemije Hermann Staudinger 1922.
Polimerna zavojnica može se promatrati kao zapetljana nit koja je nastala slučajnim odmotavanjem svitka oko prostorije. Ovaj zamka sustavno mijenja svoju konformaciju, to je prostorna konfiguracija makromolekule. Slično je putanju Brownian pokreta.
Ova zavojnica nastaje zbog činjenice da na određenoj udaljenosti polimerni lanac "gubi" informacije o smjeru. Razgovarajte o zavojnice mogu biti u slučaju kada su velike molekularne spojeve u duljini će biti puno duža od dužine strukturnih fragmenata.

Globularna konfiguracija
Makromolekula je gusta konformacija u kojoj se može usporediti volumni udio polimera s jedinicom. Globularno stanje se ostvaruje u onim slučajevima kada se međusobno privlači između pojedinih veza polimera jedan s drugim i vanjskog okruženja.
Replika strukture makromolekula je onaj dio vode koji je izgrađen kao element takve strukture. To je najbliže hidratizirano okruženje makromolekule.

Karakteristike proteinske molekule
Makromolekule proteina su hidrofilne tvari. Kada se otopi u vodi, suhi protein, u početku se proguta, onda se postupno prelazi u otopinu. Tijekom bubrenja molekule vode ulaze u unutrašnjost proteina, povezujući njegovu strukturu s polarnim skupinama. U tom slučaju, blisko pakiranje polipeptidnog lanca je labav. Obrnuta molekula proteina smatra se inverznim rješenjem. Uz naknadnu apsorpciju molekula vode, proteinske molekule se odvajaju od ukupne mase, a proces otapanja također se odvija.
No, oteklina proteinske molekule u svim slučajevima ne uzrokuje otapanje. Na primjer, kolagena nakon apsorpcije molekula vode ostaju u stanju natečene.

Teorija hidrata
Makromolekularni spojevi ovog teorijskog nije jednostavno adsorbira, elektrostatički vezivanje događa s polarnim molekulama vode, fragmenti aminokiselinskih bočnih radikalima koji imaju negativan naboj, kao osnovne aminokiseline koje nose pozitivni naboj.
Djelomično hidrirana voda vezana je peptidnim skupinama koje tvore vodikove veze s vodenim molekulama.
Na primjer, polipeptidi koji nemaju polarnih bočnih skupina bubre. Kada je vezan za peptidne skupine, dijeli polipeptidne lance. Prisutnost međulančanih mostova ne dopušta da se proteinske molekule u potpunosti otmu i prođu u obliku otopine.
Struktura makromolekula razgrađuje se kada se zagrijava, što dovodi do pucanja i oslobađanja polipeptidnih lanaca.

Značajke želatine
Prema kemijskom sastavu želatina je slična kolagenu, tvori viskoznu tekućinu s vodom. Među karakterističnim svojstvima želatine može se razlikovati njegova sposobnost stvaranja gela.
Takvi tipovi molekula se koriste kao hemostatički i agensi za zamjenu plazme. Sposobnost želatine da stvara gelove koristi se u proizvodnji kapsula u farmaceutskoj industriji.
Singularnost topljivosti makromolekula
Ove vrste molekula imaju različitu topljivost u vodi. Određuje se aminokiselinskim pripravkom. U prisutnosti polarnih aminokiselina u strukturi, sposobnost otapanja u vodi znatno se povećava.
Ova značajka također utječe i na osobitost organizacije makromolekula. u globularnih proteina veća topljivost nego u fibrilarnim makromolekulama. Tijekom brojnih eksperimenata ustanovljena je ovisnost otapanja karakteristika upotrijebljenog otapala.
Primarna struktura svake molekule proteina je različita, što daje proteinu individualnost svojstava. Prisutnost poprečnih veza između polipeptidnih lanaca smanjuje topljivost.
Primarna struktura molekula proteina je formirana zbog peptidnih (amidnih) veza, s njegovom destrukcijom dolazi do denaturacije proteina.
Isušivanje
Otopine neutralnih soli koriste se za povećanje topljivosti proteinskih molekula. Na primjer, na taj način se može provesti selektivno taloženje proteina i njihovo frakcioniranje može se provesti. Količina dobivenih molekula ovisi o početnom sastavu smjese.
Osobitost bjelančevina, koja se dobiva soljenjem, sastoji se u očuvanju bioloških svojstava nakon potpunog uklanjanja soli.
Bit procesa je uklanjanje proteina hidrata proteina od aniona i kationa soli, što osigurava stabilnost makromolekule. Maksimalni broj molekula proteina se izolira upotrebom sulfata. Ova se metoda koristi za pročišćavanje i odvajanje makromolekula proteina, jer se značajno razlikuju u veličini naboja, parametrima hidrata ljuske. Svaki protein ima svoju zasebnu solju, tj. Treba odabrati sol određene koncentracije.

Amino kiseline
Danas je poznato oko dvije stotine aminokiselina koje su dio molekula proteina. Ovisno o strukturi, oni su podijeljeni u dvije skupine:
- Proteinogeni, koji su dio makromolekula;
- ne-proteinogenog, ne sudjelujući u formiranju proteina.
Znanstvenici su uspjeli dešifrirati slijed aminokiselina u mnogim molekulama proteina životinjskog i biljnog podrijetla. Među aminokiselinama, koje se često nalaze u proteinskim molekulama, zabilježimo serin, glicin, leucin, alanin. Svaki prirodni biopolimer karakterizira vlastiti aminokiselinski sastav. Na primjer, protamini uključuju oko 85 posto arginina, ali nemaju kisele, cikličke aminokiseline. Fibroin je molekula bjelančevina prirodne svile, koja sadrži oko polovicu glicina. U kolagenu postoje takve rijetke aminokiseline kao hidroksiprolin, hidroksilizin, odsutan u drugim makrocolekulama proteina.
Aminokiselinski sastav se određuje ne samo značajke aminokiselina, ali također funkcionira, imenovanje proteina makromolekula. Njihov slijed određen je genetskim kodom.
Razine strukturne organizacije biopolimera
Postoje četiri razine: osnovna, sekundarna, tercijarna i kvartarna. Svaka struktura ima svoje osobitosti.
Primarna struktura molekula proteina je linearni polipeptidni lanac aminokiselinskih ostataka povezanih peptidnim vezama.
To je ova struktura koja je najstabilnija jer sadrži peptidne kovalentne veze između karboksilne skupine jedne aminokiseline i amino skupine druge molekule.
Sekundarna struktura uključuje polaganje polipeptidnog lanca uz pomoć vodikovih veza u spiralnom obliku.
Tercijarni tip biopolimera dobiva se prostornom pakovanju polipeptida. Podijeljeni su spiralni i laminirani savijeni oblici tercijarnih struktura.
Za globularne proteine karakterizira elipsoidni oblik, a za fibrilarne molekule ima izduženi oblik.
Ako makromolekula sadrži samo jedan polipeptidni lanac, protein ima samo tercijarnu strukturu. Na primjer, to je protein mišićnog tkiva (mioglobin), potreban za vezanje kisika. Neki biopolimeri su izgrađeni od nekoliko polipeptidnih lanaca, od kojih svaki ima tercijarnu strukturu. U ovom slučaju, makromolekula ima kvaternu strukturu koja se sastoji od nekoliko globula, ujedinjenih u velikom strukturom. Hemoglobin se može smatrati jednim kvaternarnim proteinom koji sadrži oko 8 posto histidina. To je aktivni intracelularni pufer u eritrocitima, koji omogućuje održavanje pH vrijednosti krvi na stabilnoj razini.
Nukleinske kiseline
Oni su visoki molekularni spojevi, koji su formirani od fragmenata nukleotida. RNA i DNA nalaze se u svim živim stanicama, obavljaju funkciju skladištenja, prijenosa, kao i implementaciju nasljednih informacija. Monomeri su nukleotidi. Svaki od njih ima u sastavu ostatak dušične baze, ugljikohidrata i fosforne kiseline. Istraživanja su pokazala da se načelo komplementarnosti promatra u DNA različitih živih organizama. Nukleinske kiseline su topive u vodi, ali se ne otapaju u organskim otapalima. Ovi biopolimeri uništavaju se kada se temperatura podigne, ultraljubičasto zračenje.
Umjesto zaključivanja
Uz različite proteine i nukleinske kiseline, makromolekule su ugljikohidrati. Polisaharidi u svom sastavu imaju stotine monomera, koji imaju ugodan slatki okus. Kao primjeri hijerarhijske strukture makromolekula može se navesti ogromne molekule proteina i nukleinskih kiselina s kompleksnim podjedinicama.
Na primjer, prostorna struktura globularne molekule proteina posljedica je hijerarhijske višerazinske organizacije aminokiselina. Između pojedinih razina postoji bliska veza, elementi viših razina povezani su s nižim slojevima.
Svi biopolimeri imaju važnu sličnu funkciju. Oni su građevni blokovi za žive stanice, odgovorni su za pohranu i prijenos nasljednih informacija. Za svako živo stvorenje karakteristični su specifični proteini, pa se biokemičari suočavaju s kompleksnim i odgovornim zadatkom, rješavajući što, spasavaju žive organizme od određene smrti.
 Struktura ljudske DNK
Struktura ljudske DNK Koja je veličina molekula? Koje su dimenzije molekule?
Koja je veličina molekula? Koje su dimenzije molekule? Koji je spoj monomer škroba?
Koji je spoj monomer škroba? Triplet je funkcionalna jedinica informacija u ćeliji
Triplet je funkcionalna jedinica informacija u ćeliji Protein kvartarne strukture: značajke strukture i funkcioniranja
Protein kvartarne strukture: značajke strukture i funkcioniranja Koja je razlika između DNA i RNA?
Koja je razlika između DNA i RNA? Kemijski sastav živih organizama u smislu znanosti
Kemijski sastav živih organizama u smislu znanosti Od aminokiselinskih ostataka molekula onoga što se gradi?
Od aminokiselinskih ostataka molekula onoga što se gradi? Što se sastoji od proteina? Primjeri jednostavnih i složenih proteina
Što se sastoji od proteina? Primjeri jednostavnih i složenih proteina Struktura i funkcija DNA i RNA (tablica)
Struktura i funkcija DNA i RNA (tablica) Struktura aminokiselina. Određivanje i klasifikacija aminokiselina
Struktura aminokiselina. Određivanje i klasifikacija aminokiselina Polikondenzacija je ... Reakcija polikondenzacije: primjer, svojstva i prijem
Polikondenzacija je ... Reakcija polikondenzacije: primjer, svojstva i prijem Čimbenici koji određuju topivost proteina. Fizikalno-kemijska svojstva proteina
Čimbenici koji određuju topivost proteina. Fizikalno-kemijska svojstva proteina Fibrilarni i globularni protein, protein monomer, uzorci sinteze proteina
Fibrilarni i globularni protein, protein monomer, uzorci sinteze proteina Protein: probava u tijelu
Protein: probava u tijelu DNA molekula: razine strukturne organizacije
DNA molekula: razine strukturne organizacije Deoksiribonukleinska kiselina. Model Crick i Watson
Deoksiribonukleinska kiselina. Model Crick i Watson Najveće ćelije organske tvari
Najveće ćelije organske tvari Proteini mlijeka i hidroliza proteina
Proteini mlijeka i hidroliza proteina Važnost proteina u ljudskom tijelu
Važnost proteina u ljudskom tijelu Globularni protein: struktura, struktura, svojstva. Primjeri globularnih i fibrilarnih proteina
Globularni protein: struktura, struktura, svojstva. Primjeri globularnih i fibrilarnih proteina
 Koja je veličina molekula? Koje su dimenzije molekule?
Koja je veličina molekula? Koje su dimenzije molekule? Koji je spoj monomer škroba?
Koji je spoj monomer škroba? Triplet je funkcionalna jedinica informacija u ćeliji
Triplet je funkcionalna jedinica informacija u ćeliji Protein kvartarne strukture: značajke strukture i funkcioniranja
Protein kvartarne strukture: značajke strukture i funkcioniranja Koja je razlika između DNA i RNA?
Koja je razlika između DNA i RNA? Kemijski sastav živih organizama u smislu znanosti
Kemijski sastav živih organizama u smislu znanosti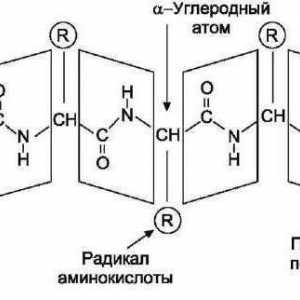 Od aminokiselinskih ostataka molekula onoga što se gradi?
Od aminokiselinskih ostataka molekula onoga što se gradi? Što se sastoji od proteina? Primjeri jednostavnih i složenih proteina
Što se sastoji od proteina? Primjeri jednostavnih i složenih proteina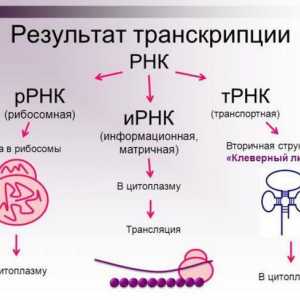 Struktura i funkcija DNA i RNA (tablica)
Struktura i funkcija DNA i RNA (tablica) Struktura aminokiselina. Određivanje i klasifikacija aminokiselina
Struktura aminokiselina. Određivanje i klasifikacija aminokiselina