Agregatno stanje materije
Fizičko ili agregatno stanje tvari karakterizira njegova specifična svojstva u specifičnim uvjetima (tlak i temperatura). To jest, može biti čvrsta, tekućina ili plinovita. Promjena agregatnih stanja tvari dovodi do promjene u njegovu fizička svojstva
sadržaj
Na primjer, agregatno stanje vode može biti čvrsta, tekućina ili plinovita. U ovom slučaju, kemijska formula (H20) i sastav molekule (dva vodikova atoma i jedan atom kisika) se ne mijenjaju. Pri temperaturama od 0 ° C i ispod je u čvrstom stanju i naziva se led. Od 0 ° C do 99.944 ° C je bezbojna (na manje količine) se prozirna tekućina, bez mirisa i okusa. Na temperaturi od 99.944 ° C prolazi se u plinsku fazu i poziva se vodene pare. Ovaj primjer pokazuje da se agregatno stanje tvari mijenja s promjenom vanjskih uvjeta. U tom slučaju, s gotovo nepromijenjenim okolnim tlakom, ali s promjenom temperature, led se topi na 0 ° C i pretvara u vodu, koja se vreli na 99.944 ° C i isparava u paru.
Voda, možemo reći, razlikuje se po svojim svojstvima, biti u različitim agregatnim stanjima. Gustoća leda jednaka je 0,917 g / cmup3, tekuća voda u standardnim uvjetima od 0,9982 g / cmup3-, vodena para (također pod standardnim uvjetima) - manja od 0,001 g / cmup3-. Dinamička viskoznost voda pri točki taljenja leda (točka smrzavanja vode) je: mi- = 1,793middot-Pamiddot 103-a, i na 20 ° C dinamičkog viskoziteta vode: mu- = 1.003middot-10ˉsup3-Pamiddot-s. Dakle, agregatno stanje tvari i njegova svojstva se mijenjaju tijekom faze prijelaza. Ovaj prijelaz karakterizira točka taljenja (od čvrste tvari postaje tekućina) jednaka temperaturi kristalizacije (tekućina se skrutne) i vrelišta (tekućina prolazi u plin) jednaka temperaturi kondenzacije (plin postaje tekućina).
Treba naglasiti da agregatno stanje tvari ovisi o njegovom sastavu. Tako, na primjer, pod istim vanjskim uvjetima, različite tvari se razlikuju po njihovim svojstvima. Pod standardnim uvjetima H2O vode je tekućina. Vodik H2 i kisik O2 su plinovi. Iron Fe je čvrsta (njegova talište 1538.9 ° C, vrelište 2860.9 ° C). Ali isto agregatno stanje za različite tvari može imati neke sličnosti.
Na primjer, relativno male intermolekularne sile karakteristične su za plinove. Stoga su njihove molekule na velikoj udaljenosti jedna od druge. Kao rezultat, plinovi mogu snažno ugovoriti. Molekule plinova se stalno kreću, a kretanje je kaotično. To je ono što objašnjava sposobnost plinovitih tvari ispuniti cijeli volumen ravnomjerno, pod uvjetom da: Plinovi uzeti oblik i volumen posude u kojoj se nalaze.
Tekućine između plinovitih i krutih tvari zauzimaju srednji položaj. Kako se temperatura diže, oni postaju više poput plinova, a uz smanjenje temperature, oni su više slični krutinama. Molekule tekućine su gusto smještene zbog znatnih sila privlačenja između njih. Röntgenske studije su pokazale da imaju neke osnove koji nalikuju kristalnoj strukturi.
Čvrste tvari uvijek imaju određene oblike i volumene. Da biste ih promijenili, potrebno je trošiti napor, budući da su molekule, atomi i ioni čvrsto povezani. Čestice čvrste tvari se ne mogu slobodno kretati, jer zadržavaju međusobno uređenje i izvode naređene oscilacije oko središta ravnoteže. Poznate su dvije čvrste tvari - amorfne i kristalne. Kristali potonje karakteriziraju oblik za njih. Na primjer, kristali natrijevog klorida NaCl nalikuju obliku kocke, kalijevog nitrata KNO3 - prizmu i tako dalje. Struktura amorfnih je slučajno agregirane molekule. Za razliku od kristalnih tvari, koji se rastopiti pri određenoj temperaturi, amorfni karakterizira širok raspon točke topljenja. Ponekad se tretiraju kao tekućina s vrlo visokom viskoznošću. Kada se uvjeti pod kojima se tvar miješa mijenjaju, može se dobiti i u kristaliničnom iu amorfnom stanju.
Agregatno stanje tvari ponekad se opisuje kao plazma ili tekući kristali. Ali to nije sasvim ispravna definicija. Ovo pitanje zahtijeva zasebnu i detaljniju studiju, tako da u ovom članku to stanje materije ne utječe.
 Kako se nalaze čestice u krutinama, tekućinama i plinovima?
Kako se nalaze čestice u krutinama, tekućinama i plinovima? Što se sastoji od vode: od kojih molekule i atomi
Što se sastoji od vode: od kojih molekule i atomi Plin je ...? Svojstva, osobine, zanimljive činjenice
Plin je ...? Svojstva, osobine, zanimljive činjenice Alotropne modifikacije kisika: komparativna svojstva i vrijednost
Alotropne modifikacije kisika: komparativna svojstva i vrijednost Fizička svojstva aldehida
Fizička svojstva aldehida Što je agregatno stanje? Agregatno stanje materije
Što je agregatno stanje? Agregatno stanje materije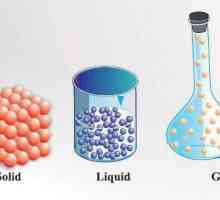 Svojstva i struktura plinovitih, tekućih i čvrstih tijela
Svojstva i struktura plinovitih, tekućih i čvrstih tijela Fizička svojstva
Fizička svojstva Viskoznost vode
Viskoznost vode Kako se tvari prelaze iz tekućeg stanja u čvrsto stanje?
Kako se tvari prelaze iz tekućeg stanja u čvrsto stanje? Tekući vodik: svojstva i primjene
Tekući vodik: svojstva i primjene Vrste tvari: tvari, fizičko polje, fizički vakuum. Koncept materije
Vrste tvari: tvari, fizičko polje, fizički vakuum. Koncept materije Fizička vrijednost: toplina isparavanja vode
Fizička vrijednost: toplina isparavanja vode Tekući helij: svojstva i svojstva tvari
Tekući helij: svojstva i svojstva tvari Struktura materije
Struktura materije Fizička svojstva vode
Fizička svojstva vode Sjećamo se fizike - kakav je toplinski kapacitet vode?
Sjećamo se fizike - kakav je toplinski kapacitet vode? Molekularna fizika
Molekularna fizika Količina topline nije tako jednostavna
Količina topline nije tako jednostavna Savršeni plin
Savršeni plin Koeficijent difuzije je gdje i koliko
Koeficijent difuzije je gdje i koliko
 Što se sastoji od vode: od kojih molekule i atomi
Što se sastoji od vode: od kojih molekule i atomi Plin je ...? Svojstva, osobine, zanimljive činjenice
Plin je ...? Svojstva, osobine, zanimljive činjenice Alotropne modifikacije kisika: komparativna svojstva i vrijednost
Alotropne modifikacije kisika: komparativna svojstva i vrijednost Što je agregatno stanje? Agregatno stanje materije
Što je agregatno stanje? Agregatno stanje materije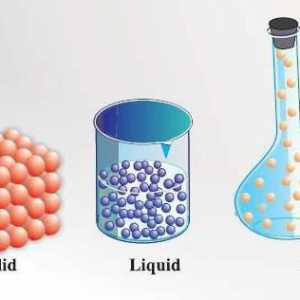 Svojstva i struktura plinovitih, tekućih i čvrstih tijela
Svojstva i struktura plinovitih, tekućih i čvrstih tijela Kako se tvari prelaze iz tekućeg stanja u čvrsto stanje?
Kako se tvari prelaze iz tekućeg stanja u čvrsto stanje? Tekući vodik: svojstva i primjene
Tekući vodik: svojstva i primjene