Što su alifatski ugljikovodici?
Alifatski ugljikovodici su organskih spojeva,
sadržaj

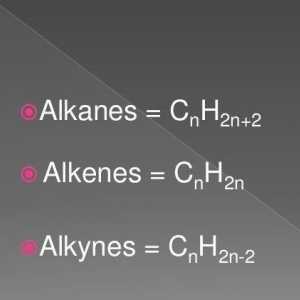
Opća formula alkana
Predstavnici ove klase karakterizirani su općom formulom CnH2n + 2. Parafini uključuju sve spojeve koji imaju otvoreni lanac, pri čemu su atomi povezani jednostavnim vezama. Zbog činjenice da su u normalnim uvjetima alifatski ugljikovodici nisko aktivni spojevi, dobili su ime "parafini". Razjasnit ćemo neke značajke strukture predstavnika ove klase, prirodu veze u molekulama, područje primjene.

Kratak opis metana
Kao najjednostavniji predstavnik ovog razreda možemo spomenuti metan. On je taj koji započinje alifatsku seriju ugljikovodika. Otkrivamo njegove osebujne osobine.
Metan je, u normalnim uvjetima, plinovita tvar koja je bez mirisa i bezbojna. Taj spoj nastaje u prirodi razgradnjom bez prisutnosti kisika zraka životinja i biljnih organizama. Na primjer, nalazi se u prirodnom plinu, pa se danas u velikim količinama koristi kao gorivo u proizvodnji iu svakodnevnom životu.
Koje vrste kemijske veze imaju ove ugljikovodike? Alifatični, ograničavajući organski spojevi su kovalentne polarne molekule.
Molekula ima tetraedrijski oblik metan molekulu, tip hibridizacije atoma ugljika u sp3, što odgovara istezanje kut 109 stupnjeva 28 minuta. Iz tog razloga alifatski ugljikovodici su kemijski nisko aktivni spojevi.

Značajke metanskih homologa
Uz metan, drugi ugljikovodici sadržani su u prirodnom plinu i ulju, koji imaju sličnu strukturu s njim. Prva četiri predstavnika homologne serije parafina su u plinovitom agregatnom stanju, imaju neznatnu topljivost u vodi.
Kako se vrijednost povećava relativna molekulska masa opaženo je povećanje točke ključanja i topljenja CxHy. Između pojedinih predstavnika serije postoji određena razlika CH2, koja se naziva homološka razlika. To je izravna potvrda povezanosti spoja s ovom organskom serijom.
Svi alifatski ugljikovodici su tvari koje su lako topljive organskih otapala.

Izomerizam serije
Za predstavnike brojnih parafina, izomerizam ugljikovog kostura je karakterističan. To je objašnjeno mogućnošću prostornog rotacije ugljikovog atoma oko kemijskih veza. Na primjer, za spajanje sastava C4H10, možete uzeti ugljikovodik ravnim ugljikovim kosturom - butanom. Kao strukturni izomer će biti 2-metilpropan, koji ima razgranatu strukturu.
Među tipičnim kemijskim svojstvima karakterističnim za parafine potrebno je napomenuti supstitucijsku reakciju. Zasićenost veza objašnjava kompleksnost reakcije, njegov radikalni mehanizam. Da bi se dobili halogenirani derivati alifatskih ugljikovodika, potrebno je provesti reakciju halogeniranja u prisustvu UV zračenja. Lančana priroda ove interakcije opažena je u svim predstavnicima ove serije. Dobiveni proizvodi se nazivaju halogenim derivatima. Oni su naširoko koristi u kemijskoj industriji kao organskih otapala.
Osim toga, svi alifatski i aromatski ugljikovodici spaljuju u prisutnosti kisika, tvoreći vodu i ugljični dioksid. Ovisno o postotnom sadržaju u molekuli ugljika, druga količina topline se oslobađa. Bez obzira na pripadnost klasi organskih spojeva, svi procesi izgaranja su egzotermne reakcije, koje se koriste u svakodnevnom životu i industriji.
Dehidrogenacija metana (cijepanje vodikom) također ima praktičnu primjenu. Kao rezultat ovog postupka, nastaje acetilen, koji je vrijedna kemijska sirovina.

Upotreba alkana i klorirani alkani
Diklormetan, kloroform i tetraklormetan su tekućine koje su izvrsna organska otapala. Kloroform i jodoform se koriste u suvremenoj medicini. Razgradnja metana jedan je od industrijskih metoda proizvodnje čađe, što je neophodno za proizvodnju tiskarske tinte. Metan se smatra glavnim izvorom proizvodnje plinovitog vodika u kemijskoj industriji, koji vodi proizvodnju amonijaka, kao i sintezi brojnih organskih tvari.
Nezasićeni ugljikovodici
Nezasićeni alifatski ugljikovodici predstavljaju brojni etilen i acetilen. Neka nam analiziramo njihova osnovna svojstva i aplikacije. Alkene su karakterizirane prisutnošću dvostruke veze, tako da opća formula za seriju ima oblik CnH2n.
S obzirom na nezasićenu prirodu tih tvari, može se primijetiti da oni ulaze u reakcijski spojevi: hidrogeniranje, halogeniranje, hidratacija, hidroliza. Osim toga, predstavnici brojnih etilena su sposobni za polimerizaciju. Upravo ta osobina čini predstavnicima ove klase zahtjevima u suvremenoj kemijskoj proizvodnji. Polietilen i polipropilen su tvari koje čine osnovu industrije polimera.
Acetilen je prvi predstavnik serije opće formule CnH2n-2. Među prepoznatljivim značajkama tih spojeva, može se izdvojiti prisutnost trostruke veze. Njegova prisutnost objašnjava tijek reakcija spoja s halogenom, vodom, vodikovim halidom, vodikom. Ako je trostruka veza u takvim spojevima smještena u prvom položaju, tada je za alkine kvalitativna supstitucijska reakcija s kompleksnom srebrnom soli karakteristična. To je ta sposobnost koja je kvalitativna reakcija na alkin, koja se koristi za otkrivanje u smjesi s alkenom i alkanom.
Aromatski ugljikovodici su ciklički nezasićeni spojevi, stoga se ne smatraju alifatskim spojevima.

zaključak
Unatoč razlikama u kvantitativnom sastavu predstavnika ograničavajućih i nezasićenih alifatskih spojeva, oni su slični u kvaliteti, sadrže ugljik i vodik u molekulama. Razlike u kvantitativnom sastavu (različite opće formule) u predstavnicima zasićenih i nezasićenih CCl2 objašnjavaju razliku u mehanizmima reakcija dobivanja različitih proizvoda.
Zato su pripadnici svih klasa tih spojeva ući u reakciju izgaranja u obliku ugljičnog dioksida, vode, dodjeljivanjem određenu količinu toplinske energije, što ih čini popularan kao gorivo u svakodnevnom životu i industrije.
 Razvrstavanje organskih tvari - osnova za proučavanje organske kemije
Razvrstavanje organskih tvari - osnova za proučavanje organske kemije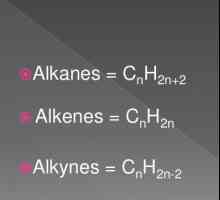 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena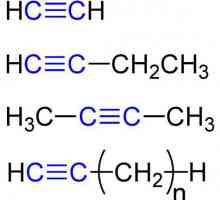 Kemijska svojstva alkina. Struktura, prijem, primjena
Kemijska svojstva alkina. Struktura, prijem, primjena Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Kako napraviti izomere i homologe? Kako napraviti izomere alkana? Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane Aromatski ugljikovodici: glavni predstavnici i njihova primjena u nacionalnom gospodarstvu.
Aromatski ugljikovodici: glavni predstavnici i njihova primjena u nacionalnom gospodarstvu.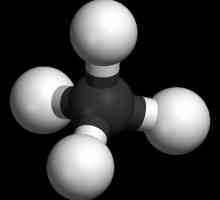 Alkadieni su tipični predstavnici nezasićenih ugljikovodika
Alkadieni su tipični predstavnici nezasićenih ugljikovodika Koja je strukturna formula izoprena
Koja je strukturna formula izoprena Što su aromatski ugljikovodici: formula, svojstva
Što su aromatski ugljikovodici: formula, svojstva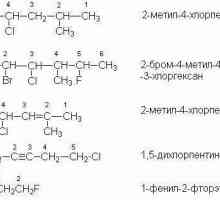 Što je sustavna nomenklatura
Što je sustavna nomenklatura Pentan: izomeri i nomenklatura
Pentan: izomeri i nomenklatura Zasićeni ugljikovodici: svojstva, formule, primjeri
Zasićeni ugljikovodici: svojstva, formule, primjeri Organski spojevi i njihova klasifikacija
Organski spojevi i njihova klasifikacija Kemijska svojstva alkana
Kemijska svojstva alkana Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva
Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva Serije homologije
Serije homologije Diene ugljikovodici: struktura, izomerizam i nomenklatura
Diene ugljikovodici: struktura, izomerizam i nomenklatura Alkanes: kemijska svojstva
Alkanes: kemijska svojstva Kemijska svojstva alkena (olefina)
Kemijska svojstva alkena (olefina) Izomeri heptana: opća karakteristika i primjena
Izomeri heptana: opća karakteristika i primjena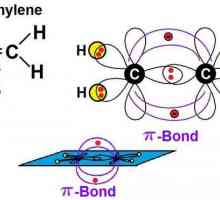 Alkeni: formula. Kemijska svojstva. recepcija
Alkeni: formula. Kemijska svojstva. recepcija
 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena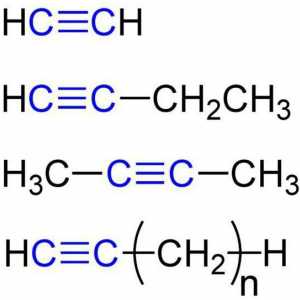 Kemijska svojstva alkina. Struktura, prijem, primjena
Kemijska svojstva alkina. Struktura, prijem, primjena Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Kako napraviti izomere i homologe? Kako napraviti izomere alkana? Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane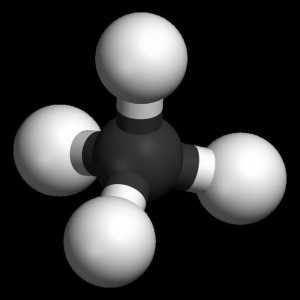 Alkadieni su tipični predstavnici nezasićenih ugljikovodika
Alkadieni su tipični predstavnici nezasićenih ugljikovodika Koja je strukturna formula izoprena
Koja je strukturna formula izoprena Što su aromatski ugljikovodici: formula, svojstva
Što su aromatski ugljikovodici: formula, svojstva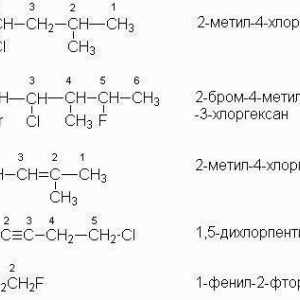 Što je sustavna nomenklatura
Što je sustavna nomenklatura Pentan: izomeri i nomenklatura
Pentan: izomeri i nomenklatura