Anorganske tvari
Anorganske tvari su kemijski spojevi koji za razliku od organskih tvari ne sadrže ugljik (osim cijanida, karbida, oksidi ugljika,
sadržaj
Klasifikacija anorganskih tvari je sljedeća. Je jednostavna stvar: nemetala (H2, N2, O2), metala (Na, Zn, Fe), amfoterni jednostavne supstance (Mn, Zn, Al), plemeniti plinovi (Xe On, RN) i složene tvari oksida (H2O, CO2, P2O5) - hidroksid (Ca (OH) 2, H2SO4) - soli (CuSO4, NaCl, KNO3, Ca3 (PO4) 2), binarni spoj.
Molekule jednostavnih (jednostrukih) tvari sastoje se samo od atoma određene (jedne) vrste (elementa). Oni se ne raspadaju u kemijskim reakcijama i nisu sposobni formirati druge tvari. Jednostavne tvari zauzvrat su podijeljene na metale i nefemale. Jasne granice između njih ne postoje zbog sposobnosti jednostavnih tvari da dokažu dvostruka svojstva. Neki elementi istodobno pokazuju svojstva oba metala i nemetala. Pozvani su amfoterni.
Plemeniti plinovi su anorganske tvari zasebne klase - oni ističu među ostalima na osebujan način. To su elementi VIIIA skupina.
Sposobnost nekih elemenata da oblikuju nekoliko jednostavnih, različite strukture i svojstava, zove se alotropija. Primjeri mogu biti elementi C, karbid dijamantni oblik i grafit - O - ozon i kisik - P - bijeli, crveni, crni i drugi. Ova pojava je moguća zbog različitog broja atoma u molekuli i zbog sposobnosti atoma da oblikuju različite kristalne oblike.
Pored jednostavnih osnovnih klasa anorganskih tvari uključuju se kompleksni spojevi. Pod kompleksnim (dvodimenzijskim ili višeslojnim) supstancijama podrazumijevaju se spojevi kemijskih elemenata. Njihove molekule sastoje se od atoma različitih tipova (različitih elemenata). Kada se raspadaju u kemijskim reakcijama, tvore nekoliko drugih tvari. Podijeljeni su u baze, oksidi, kiseline i soli.
U bazama, atomi metala povezani su na hidroksilne skupine (ili jednu skupinu). Ovi spojevi podijeljeni su u topljive (alkalne) i netopljive u vodi.
Oksidi se sastoje od dva elementa, od kojih je jedan kisik. Oni su ne-soli i formiraju soli.
Hidroksidi su tvari koje tvore interakcije (izravno ili neizravno) s vodom. To uključuje: baze (Al (OH) 3, Ca (OH) 2), kiseline (HCl, H2S04, HNO3, H3P04) amfoternih hidroksida (Al (OH) 3, Zn (OH) 2). U interakciji različitih tipova hidroksida, soli između kisika formiraju međusobno.
Soli su podijeljeni u mediju (sastoji se od kationa i aniona - Ca3 (PO4) 2, Na2SO4) - kiseline (u kiselinski dio sadrži vodikovim atomima koji zamijeniti kationima -NaHSO3, CaHPO4), bazičnim (sastavljeni od okso ili hydroxo - Cu2CO3 (OH) 2), - dvostruka (sadrži dvije različite reaktivne kation) i / ili kompleksa (koji sadrži dva različita kiseli ostatak) sol (CaMg (CO3) 2, K3 [Fe (CN) 6]).
Binarni spojevi (prilično velika klasa tvari) podijeljeni su na kiseline bez kisika (H2S, HCl) - soli bez kisika (CaF2, NaCl) i drugi spojevi (CaC2, AlH3, CS2).
Anorganske tvari nemaju ugljikov skelet, koji je osnova organskih spojeva.
U ljudskom tijelu postoji a Organska tvar (34%), kao i anorganski spojevi. Potonji uključuju, prije svega, vodu (60%) i kalcijeve soli, od kojih je ljudski kostur pretežno.
Anorganske tvari u ljudskom tijelu predstavljaju 22 kemijska elementa. Većina njih su metali. Ovisno o koncentraciji elemenata u tijelu, oni se nazivaju mikro- (sadržaj u tijelu koji ne prelazi 0,005% tjelesne težine) i makroelemenata. Nezamjenjivi mikroelementi za organizam jod, željezo, bakar, cink, mangan, molibden, kobalt, krom, selenij, fluor. Njihov unos hranom u tijelu nužan je za normalan život. Makro elementi poput kalcija, fosfora i klora temelj su mnogih tkiva.
 Što je složena tvar? Kako se to događa?
Što je složena tvar? Kako se to događa? Što je materija? Koje su klase tvari. Razlika između organskih i anorganskih tvari
Što je materija? Koje su klase tvari. Razlika između organskih i anorganskih tvari Organski materijal njihovih svojstava i klasifikacije
Organski materijal njihovih svojstava i klasifikacije Kvalitativne reakcije na organske tvari, anione, katione
Kvalitativne reakcije na organske tvari, anione, katione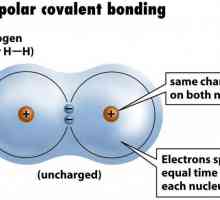 Primjer nepolarne kovalentne veze. Kovalentna veza polarna i nepolarna
Primjer nepolarne kovalentne veze. Kovalentna veza polarna i nepolarna Kemija: oksidi, njihova klasifikacija i svojstva
Kemija: oksidi, njihova klasifikacija i svojstva Koja je priroda oksida
Koja je priroda oksida Kako odrediti kvalitativni i kvantitativni sastav tvari
Kako odrediti kvalitativni i kvantitativni sastav tvari Nemetali su ...? Svojstva ne-metala
Nemetali su ...? Svojstva ne-metala Anorganska kemija. Opća i anorganska kemija
Anorganska kemija. Opća i anorganska kemija Alkali metali
Alkali metali Organski spojevi i njihova klasifikacija
Organski spojevi i njihova klasifikacija Klase anorganskih spojeva
Klase anorganskih spojeva Jednostavne tvari
Jednostavne tvari Najveće ćelije organske tvari
Najveće ćelije organske tvari Amfoterni metali i njihova svojstva
Amfoterni metali i njihova svojstva Osnovni oksidi i njihova svojstva
Osnovni oksidi i njihova svojstva Organske i anorganske tvari
Organske i anorganske tvari Oksidi, oksidi koji formiraju natrij i koji ne stvaraju soli
Oksidi, oksidi koji formiraju natrij i koji ne stvaraju soli Kemijska svojstva soli i postupci za njihovo dobivanje
Kemijska svojstva soli i postupci za njihovo dobivanje Anorganske tvari: primjeri i svojstva
Anorganske tvari: primjeri i svojstva
 Što je materija? Koje su klase tvari. Razlika između organskih i anorganskih tvari
Što je materija? Koje su klase tvari. Razlika između organskih i anorganskih tvari Kvalitativne reakcije na organske tvari, anione, katione
Kvalitativne reakcije na organske tvari, anione, katione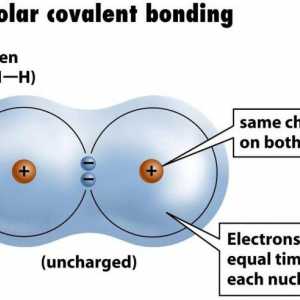 Primjer nepolarne kovalentne veze. Kovalentna veza polarna i nepolarna
Primjer nepolarne kovalentne veze. Kovalentna veza polarna i nepolarna Kemija: oksidi, njihova klasifikacija i svojstva
Kemija: oksidi, njihova klasifikacija i svojstva Koja je priroda oksida
Koja je priroda oksida Kako odrediti kvalitativni i kvantitativni sastav tvari
Kako odrediti kvalitativni i kvantitativni sastav tvari Nemetali su ...? Svojstva ne-metala
Nemetali su ...? Svojstva ne-metala Anorganska kemija. Opća i anorganska kemija
Anorganska kemija. Opća i anorganska kemija