Kako napraviti izomere i homologe? Kako napraviti izomere alkana?
Prije analize kako napraviti izomere ograničavajući ugljikovodike,
sadržaj
Zasićeni ugljikovodici
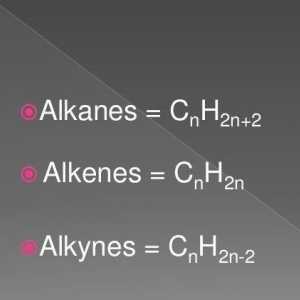
U organskoj kemiji se razlikuju mnoge klase CxHy. Svaka ima svoju opću formulu, homološke serije, kvalitativne reakcije, primjena. za zasićene ugljikovodike klasični alkani karakterizirani su jednim (sigma) vezama. Opća formula za ovu klasu organskih tvari je CnH2n + 2. Ovo objašnjava glavna kemijska svojstva: zamjena, izgaranje, oksidacija. Parafini nisu karakterizirani dodavanjem, jer su veze u molekulama tih ugljikovodika pojedinačne.

izomera
Takav fenomen kao i izomerizam objašnjava raznolikost organskih tvari. Pod izomerizmom je uobičajeno razumjeti fenomen u kojem postoji nekoliko organskih spojeva, s istim kvantitativnim sastavom (broj atoma u molekuli), ali njihov različit raspored u molekuli. Rezultirajuće tvari nazivaju se izomeri. Oni mogu biti predstavnici nekoliko klasa ugljikovodika i stoga se razlikuju po kemijskim svojstvima. Različiti spojevi u molekuli alkana C atoma dovode do pojave strukturnih izomerizma. Kako napraviti izomere alkana? Postoji određeni algoritam prema kojem je moguće prikazati strukturne izomere određene klase organskih tvari. Postoji slična mogućnost s samo četiri atoma ugljika, tj. S butanskom molekulom C4H10.
Vrste izomerizma
Da bismo razumjeli kako napraviti izomere, važno je imati ideju o njegovim oblicima. Ako postoje jednaki atomi unutar molekule u jednakim količinama, koji se nalaze u prostoru različitog reda, govorimo o prostornom izomerizmu. Inače se naziva stereoizomerizam. U takvoj situaciji sama upotreba strukturnih formula neće biti dovoljna, bit će potrebno koristiti posebne projekcijske ili prostornu formulu. Ograničavajući ugljikovodici, počevši od H3C-CH3 (etana), imaju različite prostorno oblikovanje. To je zbog rotacije unutar molekule kroz C-C vezu. To je jednostavno sigma - komunikacija stvara konformacijski (rotirajući) izomerizam.

Strukturni izomerizam parafina
Razgovarajmo o tome kako napraviti izomere alkana. Klasa ima strukturni izomerizam, tj. Ugljikov atom tvori različite lance. Inače, mogućnost promjene položaja u lancu ugljikovih atoma naziva se izomerizam ugljikovog kostura.

Izomeri heptana
Dakle, kako ostaviti izomere za tvar koja ima sastav C7H16? Za početak, možete organizirati sve ugljikove atome u jednom dugom lancu, dodati određeni broj atoma C svaki. Koliko? S obzirom da je valencija ugljika četiri, najudaljeniji atomi imat će tri atoma vodika, a unutarnji atomi imaju dva vodikova atoma. Dobivena molekula ima linearnu strukturu, takav ugljikovodik se naziva n-heptan. Slovo "n" podrazumijeva ravni ugljikov skelet u ovom ugljikovodiku.
Sada promijenimo raspored ugljikovih atoma, "skraćivanje" ravnog ugljikovog lanca u C7H16. Moguće je sastaviti izomere u proširenom ili skraćenom strukturnom obliku. Razmotrite drugu opciju. Prvo, organizujemo jedan C atom u obliku metilnog radikala u različitim položajima.
Ovaj izomer heptana ima sljedeće kemijsko ime: 2-metilheksan. Sada "rad" prebacujemo na sljedeći ugljikov atom. Dobiveni ograničeni ugljikovodik se zove: 3-metilheksan.
Ako nastavimo kretanje radikala, brojanje počinje s desne strane (ugljikovodik radikal je bliži početku), tj. Dobit ćemo jedan izomer koji već imamo. Stoga, razmišljamo o tome kako napraviti izomere formule za izvornu tvar, pokušajmo da kostur bude čak "kraći".
Preostala dva ugljika mogu se prikazati kao dva slobodna radikala - metil.
Prvo ih organizujemo za različite ugljike koji ulaze u glavni lanac. Nazvat ćemo dobiveni izomer -2,3 dimetilpentana.
Sada ostavljamo jedan radikal na istom mjestu, a drugo prelazimo na sljedeći ugljikov atom glavnog lanca. Ova tvar se naziva 2,4-dimetilpentanom.
Sada uredite ugljikovodične radikale s jednog atoma ugljika. Prvo, drugo, dobivamo 2,2-dimetilpentan. Tada je treći, dobivajući 3,3 dimetilpentan.
Sada ostavljamo u glavnom lancu četiri ugljikova atoma, a preostala tri koriste kao metilni radikali. Mi ih dogovorimo kako slijedi: dva za drugi atom C, jedan za treći ugljik. Nazvat ćemo dobiveni izomer: 2,2,3 trimetilbutan.
Upotrebom primjera heptana analizirali smo kako točno napraviti izomere za krajnje ugljikovodike. Slika prikazuje primjere strukturnih izomera za buten6 njegovih derivata klora.

alkeni
Ova klasa organskih tvari ima opću formulu CnH2n. Pored zasićenih C-C veza, tu je i dvostruka veza u ovoj klasi. Određuje glavna svojstva ove serije. Razgovarajmo o tome kako napustiti izomere alkena. Pokušajmo identificirati njihove razlike od krajnjih ugljikovodika. Osim izomerije glavnog lanca (strukturne formule) za predstavnika ove klase organskih ugljikovodika karakteriziraju tri vrste izomere, geometrijske (cis i trans oblika), multipla položaj vezivanja i Interclass izomera (cikloalkani).

Izomeri C6H12
Pokušajmo saznati kako sastaviti izomere c6h12 s obzirom na činjenicu da supstanca s ovom formulom može izravno pripadati dvije klase organskih tvari: alkeni, cikloalkani.
Prvo ćemo razmotriti kako napraviti izomere alkena, ako postoji dvostruka veza u molekuli. Stavili smo ravni lanac ugljika, stavili višestruku vezu nakon prvog atoma ugljika. Pokušajmo ne samo sastaviti izomere c6n12, već i navesti tvari. Ta supstancija - heksen - 1. Slika prikazuje položaj molekule dvostruke veze. Kada se kreće uz ugljikov lanac, dobivamo heksen-2, kao i heksen-3
Sada raspravljamo o tome kako napraviti izomere za određenu formulu mijenjajući broj atoma u glavnom krugu.
Prvo skratimo ugljikov skelet na jedan atom ugljika, smatra se metilnim radikalima. Ostavimo dvostruku vezu nakon prvog atoma C. Dobiveni izomer od sustavna nomenklatura imat će sljedeće ime: 2 metilpenten - 1. Sada pomaknemo ugljikovodik radikal duž glavnog lanca, ostavljajući položaj dvostruke veze nepromijenjen. Ovaj nezasićeni ugljikovodik razgranate strukture naziva se 3-metilpenten-1.
Daljnji izomer je moguć bez promjene glavnog lanca i položaja dvostruke veze: 4 metilpenten-1.
Za sastav C6H12, možete pokušati premjestiti dvostruku vezu od prvog do drugog položaja, bez pretvaranja samog glavnog lanca. Radikal će zatim kretati duž ugljikovog kostura, počevši od drugog atoma C. Ovaj izomer naziva se 2 metilpenten-2. Osim toga, moguće je staviti radikal CH3 trećeg ugljikovog atoma, dok se dobiva 3 metilpenten-2
Ako je radikal smješten na četvrtom ugljiku atoma u danom lancu, nastaje druga nova supstancija, nezasićeni ugljikovodik s kružnim ugljenom - 4 metilpenten-2.
Uz daljnje smanjenje broja C u glavnom lancu, može se dobiti drugi izomer.
Ostavimo dvostruku vezu nakon prvog ugljikovog atoma i stavimo dva radikala na treći C atom glavnog lanca, dobivamo 3,3-dimetilen-l.
Sad stavljamo radikale blizu susjednih ugljikovih atoma, bez promjene položaja dvostruke veze, dobivamo 2,3-dimetilbuten-l. Pokušajmo, bez mijenjanja veličine glavnog lanca, premjestiti dvostruku vezu na drugu poziciju. U tom slučaju možemo smjestiti radikale samo u 2 i 3 C atoma, da se dobije 2,3-dimetilbuten-2.
Nema drugih strukturnih izomera za ovaj alken, bilo koji pokušaj da se oni s njima dovesti do kršenja teorije strukture organskih tvari AM Butlerov.

Prostorni izomeri C6H12
Sad ćemo saznati kako sastaviti izomere i homologe s gledišta prostornog izomerizma. Važno je razumjeti da su cis i trans forme alkena moguće samo za položaj dvostruke veze 2 i 3.
Kada su ugljikovodični radikali u istoj ravnini, nastaje cis-mjerenje heksen-2, a pri rasporedu radikala na različitim ravninama, trans-oblik heksena je 2.
Interklasni izomeri C6H12
Osporavajući se kako sastaviti izomere i homologe, ne treba zaboraviti na takvu mogućnost kao što je među-klasni izomerizam. za nezasićenih ugljikovodika niza etilena opće formule CnH2n, takvi su izomeri cikloalkani. Značajka ove klase ugljikovodika je prisutnost cikličke (zatvorene) strukture zasićene jednostruke veze između ugljikovih atoma. Moguće je formulirati formule cikloheksana, metilciklopentana, dimetilciklobutana, trimetilciklopropana.

zaključak
Organska kemija je višestruka, tajanstvena. Količina organskih tvari premašuje stotinu puta više anorganskih spojeva. Ta se činjenica lako objašnjava postojanjem takvog jedinstvenog fenomena kao što je izomerizam. Ako u jednoj homolognoj seriji postoje slične supstance i strukture, onda kada se položaj ugljikovih atoma u lancu mijenja, pojavljuju se novi spojevi koji se nazivaju izomeri. Tek nakon pojave teorije kemijske strukture organskih tvari bilo je moguće klasificirati sve ugljikovodike, kako bi se razumjela specifičnost svakog razreda. Jedan od prijedloga ove teorije izravno se odnosi na fenomen izomerizma. Veliki ruski kemičar bio je u mogućnosti razumjeti, objasniti, dokazati da kemijska svojstva tvari, njegova reaktivna aktivnost, praktična primjena ovise o položaju ugljikovih atoma. Ako uspoređujemo broj izomera koji nastaju ograničavanjem alkana i nezasićenih alkena, naravno, alkeni vode. To se objašnjava činjenicom da u njihovim molekulama postoji dvostruka veza. Upravo ta tvar dopušta ovoj klasi organskih tvari da formiraju ne samo alkene različitih tipova i struktura, nego i da razgovaraju o metaboličkom izomerizmu s cikloalkanima.
 Razvrstavanje organskih tvari - osnova za proučavanje organske kemije
Razvrstavanje organskih tvari - osnova za proučavanje organske kemije Organski materijal njihovih svojstava i klasifikacije
Organski materijal njihovih svojstava i klasifikacije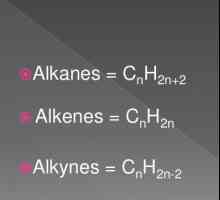 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane Alkadieni su tipični predstavnici nezasićenih ugljikovodika
Alkadieni su tipični predstavnici nezasićenih ugljikovodika Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva
Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena
Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena Što su aromatski ugljikovodici: formula, svojstva
Što su aromatski ugljikovodici: formula, svojstva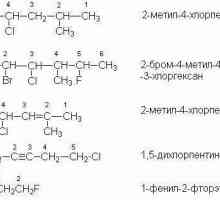 Što je sustavna nomenklatura
Što je sustavna nomenklatura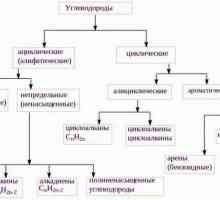 Što su alifatski ugljikovodici?
Što su alifatski ugljikovodici?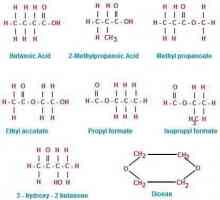 Što su strukturni izomeri
Što su strukturni izomeri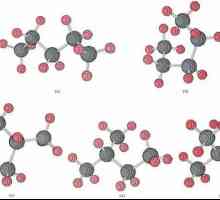 Pentan: izomeri i nomenklatura
Pentan: izomeri i nomenklatura Zasićeni ugljikovodici: svojstva, formule, primjeri
Zasićeni ugljikovodici: svojstva, formule, primjeri Organski spojevi i njihova klasifikacija
Organski spojevi i njihova klasifikacija Kemijska svojstva alkana
Kemijska svojstva alkana Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva
Ograničiti ugljikovodike: opće karakteristike, izomerizam, kemijska svojstva Serije homologije
Serije homologije Vrste izomerizma organskih tvari
Vrste izomerizma organskih tvari Alkanes: kemijska svojstva
Alkanes: kemijska svojstva Izomeri heptana: opća karakteristika i primjena
Izomeri heptana: opća karakteristika i primjena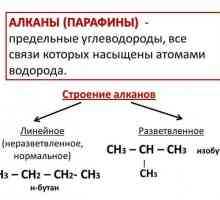 Proizvodnja alkana i njihovih svojstava
Proizvodnja alkana i njihovih svojstava
 Opća formula alkena. Svojstva i svojstva alkena
Opća formula alkena. Svojstva i svojstva alkena Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane
Ciklički zasićeni ugljikovodici: kako su proizvedeni. cikloalkane Alkadieni su tipični predstavnici nezasićenih ugljikovodika
Alkadieni su tipični predstavnici nezasićenih ugljikovodika Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva
Cikloalkani su ... Cikloalkani: priprema, formula, kemijska i fizikalna svojstva Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena
Kvalitativne reakcije na alkene. Kemijska svojstva i struktura alkena Što su aromatski ugljikovodici: formula, svojstva
Što su aromatski ugljikovodici: formula, svojstva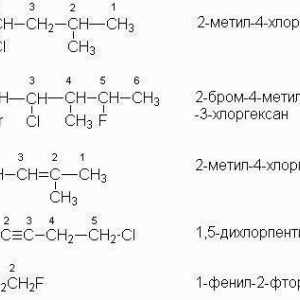 Što je sustavna nomenklatura
Što je sustavna nomenklatura Što su alifatski ugljikovodici?
Što su alifatski ugljikovodici? Što su strukturni izomeri
Što su strukturni izomeri