Struktura proteina kvaternarne strukture, svojstva sinteze i genetike
Proteini su jedan od važnih organskih elemenata bilo koje žive stanice tijela. Oni obavljaju različite funkcije: osnovni, signalni, enzimski, transportni, strukturni, receptori, itd. Važan evolucijski uređaj je primarna, sekundarna, tercijarna i kvartarna struktura proteini. Koje su
sadržaj
- Strukturne komponente proteina
- Primarna struktura proteina
- Sekundarnu strukturu proteina
- Značajke sekundarne strukture
- Tercijarna struktura
- Struktura proteina u kvarternoj strukturi molekule
- Dodatne strukture proteina
- Gdje je formirana kvaterna struktura proteinske molekule?
- Primjeri oligomernih proteina
- Hemoglobin
- Klorofil
- Hemocyanin
Strukturne komponente proteina
Monomeri bilo kojeg polipeptidnog lanca su aminokiseline (AA). Ovi nisko molekularni organski spojevi su vrlo česti prirode i mogu postojati kao nezavisne molekule, obavljajući vlastite funkcije. Među njima, prijevoz tvari, prijem, inhibicija ili aktivacija enzima.
Ukupno ima oko 200 biogenih aminokiselina, ali samo njih 20 mogu biti monomeri proteina. Oni se lako otapaju u vodi, imaju kristalnu strukturu i mnogi od njih su slatki za okus.

S kemijske točke gledišta, AK su molekule, u kojima su nužno prisutne dvije funkcionalne skupine: -COOH i -NH2. Uz pomoć ovih grupa, aminokiseline formiraju lance, koje se međusobno povezuju peptidnom vezom.
Svaka od 20 proteinogenih aminokiselina ima svoj radikal, ovisno o kemijskim svojstvima koja su različita. Što se tiče sastava takvih radikala, svi AA su razvrstani u nekoliko skupina.
- Nepolarni: izoleucin, glicin, leucin, valin, prolin, alanin.
- Polarna i nenabijena: treonin, metionin, cistein, serin, glutamin, asparagin.
- Aromatski: tirozin, fenilalanin, triptofan.
- Polar i negativno nabijen: glutamat, aspartat.
- Polar i pozitivno nabijeni: arginin, histidin, lizin.
Bilo koja razina organizacije proteinske strukture (primarna, sekundarna, tercijarna, kvaternarna) temelji se na polipeptidnom lancu koji se sastoji od AA. Jedina je razlika u tome kako se ova sekvenca razvija u prostoru i uz pomoć kojih kemijske veze održava takvu konformaciju.

Primarna struktura proteina
Bilo koji protein nastaje na ribosomima - ne-membranskim organelima stanice koja sudjeluje u sintezi polipeptidnog lanca. Ovdje su aminokiseline povezane čvrstom peptidnom vezom, tvoreći primarnu strukturu. Međutim, takva primarna struktura proteina iz kvartara je vrlo različita pa je potrebno daljnje sazrijevanje molekule.
Takvi proteini kao elastin, histoni, glutation, već s takvom jednostavnom strukturom mogu obavljati svoje funkcije u tijelu. Za veliku većinu bjelančevina sljedeći korak je stvaranje složenijih sekundarnih konformacija.

Sekundarnu strukturu proteina
Oblikovanje peptidnih veza je prva faza u sazrijevanju većine proteina. Kako bi mogli obavljati svoje funkcije, njihova lokalna konformacija mora proći neke promjene. To se postiže uz pomoć vodikovih veza - krhke, ali istovremeno i brojne veze između glavnih i kiselih centara molekula amino kiselina.
Tako nastaje sekundarna struktura proteina, od kvartara razlikuje se jednostavnost opreme i lokalne konformacije. Potonji znači da cijeli lanac ne prolazi kroz transformaciju. Vodikove veze mogu se formirati na nekoliko mjesta različitih udaljenosti od drugih, a njihov oblik ovisi io vrsti aminokiselina i načinu montaže.
Lizozim i pepsin su predstavnici proteina koji imaju sekundarnu strukturu. Pepsin je uključen u probavu, a lizozim obavlja zaštitnu funkciju u tijelu, uništavajući stanične zidove bakterija.

Značajke sekundarne strukture
Lokalne konformacije peptidnog lanca mogu se međusobno razlikovati. Već su proučavani nekoliko desetaka, a tri su najčešća. Među njima, alfa-helix, beta slojevi i beta-okret.
- Alfa-helix je jedna od često nastalih konformacija sekundarne strukture većine bjelančevina. To je kruti jezgra okvira s hodom od 0,54 nm. Radikali aminokiselina usmjereni su prema van.
Najčešće desne spirale, a ponekad i analogne lijeve strane. Oblikovanje oblika izvodi se vodikovim vezama, koje stabiliziraju kovrče. Lanac koji tvori alfa spiralu sadrži vrlo malo prolina i polarnih nabijenih aminokiselina.
- Beta rotacija se izdvaja u posebnoj konformaciji, iako se to može nazvati dijelom beta sloja. Bit leži u savijanju peptidnog lanca, koji je podržan vodikovim vezama. Obično sama zavoj sastoji se od 4-5 aminokiselina, među kojima je prisutnost prolina neophodna. Ova AK ima samo tvrdi i kratki kostur, što omogućuje stvaranje samog skretanja.
- Beta-sloj je lanac aminokiselina, koji formira nekoliko zavoja i stabilizira ih vodikovim vezama. Takva je konformacija vrlo slična presavijenom papiru. Najčešće ovaj oblik ima agresivne bjelančevine, ali postoje mnoge iznimke.
Postoje paralelni i antiparalni beta slojevi. U prvom slučaju, C i N krajevi podudaraju se na mjestima savijanja i na krajevima lanca, au drugom slučaju br.
Tercijarna struktura
Daljnje pakiranje proteina dovodi do stvaranja tercijarne strukture. Takva konformacija se stabilizira uz pomoć vodika, disulfida, hidrofobnih i ionskih veza. Njihov veliki broj omogućuje vam da zavrtite sekundarnu strukturu u složeniji oblik i stabilizirate ga.
Odvojite globularno i fibrilarnih proteina. Molekula globularnih peptida je globularna struktura. Primjeri: albumin, globulin, histoni u tercijarnoj strukturi.
Fibrilni proteini oblikuju snažne niti, čija duljina prelazi njihovu širinu. Takvi proteini najčešće izvode strukturne i funkcionalne funkcije oblikovanja. Primjeri su fibroin, keratin, kolagen, elastin.

Struktura proteina u kvarternoj strukturi molekule
Ako se nekoliko globula kombinira u jedan kompleks, stvara se takozvana kvaternarna struktura. Takva konformacija nije karakteristična za sve peptide, a formirana je kada je potrebno izvršiti važne i specifične funkcije.
Svaka globula u sastavu kompleksnog proteina je zasebna domena ili protomer. U skupini struktura proteina kvarterne strukture Molekula se naziva oligomer.
Obično takav protein ima nekoliko stabilnih konformacija koje se međusobno međusobno zamjenjuju bilo ovisno o utjecaju nekih vanjskih faktora, bilo kada je potrebno izvršiti različite funkcije.
Važna razlika između tercijarne strukture proteina i kvartera je međumolekularne veze, koje su odgovorne za kombiniranje nekoliko globula. U središtu cijele molekule često se nalazi metalni ion, koji izravno utječe na stvaranje intermolekularnih veza.
Dodatne strukture proteina
Nije uvijek niz aminokiselina dovoljan da ispuni funkcije proteina. U većini slučajeva, druge molekule organske i anorganske prirode pridružuju se takvim molekulama. Budući da je ta značajka karakteristična za veliki broj enzima, sastav složenih proteja obično se dijeli na tri dijela:
- Azenzim je proteinni dio molekule koja je aminokiselinska sekvenca.
- Koenzim nije protein nego organski dio. Može uključivati različite vrste lipida, ugljikohidrata ili čak nukleinskih kiselina. To uključuje predstavnike biološki aktivnih spojeva, među kojima postoje i vitamini.
- Cofactor je anorganski dio, koji je u većini slučajeva zastupljen metalnim ionima.
Struktura proteina u kvarternoj strukturi molekule zahtijeva sudjelovanje nekoliko molekula različitih podrijetla, tako da mnogi enzimi imaju samo tri komponente. Primjer je fosfokinaza, enzim koji osigurava prijenos fosfatne skupine iz ATP molekule.
Gdje je formirana kvaterna struktura proteinske molekule?
Lanac polipeptida počinje se sintetizirati na ribosomima stanice, ali daljnja sazrijevanje proteina već se javlja u drugim organelama. Novoformirana molekula mora pasti u transportni sustav, koji se sastoji od nuklearne membrane, EPS, Golgi aparata i lizosoma.
Povećanje složenosti prostorne strukture proteina se odvija u endoplazmatski retikulum, gdje su ne samo da se dobije različite vrste veze (vodik, disulfid, hidrofobna intermolekularno ionske), ali su se pridružili koenzim i kofaktora. To čini kvaternu strukturu proteina.
Kad je molekula potpuno spremna za rad, dolazi do citoplazme ćelije ili Golgijevog aparata. U potonjem slučaju, ovi peptidi se pakiraju u lizosome i transportiraju u druge kompartimentalne stanice.
Primjeri oligomernih proteina
Kvaternarna struktura je struktura proteina, koja je dizajnirana da olakša rad vitalnih funkcija u živom tijelu. Složena konformacija organskih molekula omogućava prije svega da utječe na rad mnogih metaboličkih procesa (enzima).
Biološki važni proteini su hemoglobin, klorofil i hemocyanin. Porfirinski prsten je osnova tih molekula, u čijem je središtu metalni ion.
hemoglobin
Kvaterna struktura molekule hemoglobinskih proteina je 4 globula povezana intermolekularnim vezama. U sredini je porfin s željeznim ionom. Protein se prenosi na citoplazmu eritrocita, gdje je zauzeto oko 80% ukupne citoplazme.
Temelj molekule je heme, koji je više anorganski u prirodi i crvene boje. Također je primarni proizvod razgradnje hemoglobina u jetri.
Svi znamo da hemoglobin obavlja važnu transportnu funkciju - prijenos kisika i ugljičnog dioksida kroz ljudsko tijelo. Složena konformacija proteinske molekule tvori posebne aktivne centre koji mogu vezati odgovarajuće plinove s hemoglobinom.
Kada se stvori kompleks "protein-plin" nastaju tzv. Oxyhemoglobin i carbogemoglobin. Međutim, postoji još jedna vrsta takvih asocijacija, koja je prilično stabilna: karboksihemoglobin. To je kompleks bjelančevina i ugljičnog monoksida, čija stabilnost objašnjava napade gušenja u slučaju pretjerane toksičnosti.

klorofil
Drugi predstavnik proteina s kvaternarnom strukturom čija je povezanost već podržana magnezij ionom. Glavna funkcija cijele molekule je sudjelovanje u procesima fotosinteze u biljkama.
Postoje različite vrste klorofila, koje se međusobno razlikuju od radikala porfirinskog prstena. Svaka od tih vrsta obilježena je zasebnim slovom latinske abecede. Na primjer, za kopnenih biljaka karakterizira prisutnost klorofil a i b, klorofil a alge nalaze u drugim vrstama proteina.

Hemocyanin
Ova molekula je analogni hemoglobin u mnogim nižim životinjama (artropodi, mekušci, itd.). Glavna razlika između strukture proteina i kvaterne strukture molekule je prisutnost cinkovog iona umjesto željeznog iona. Hemocyanin ima plavkastu boju.
Ponekad se ljudi pitaju što bi se dogodilo ako se hemoglobina osobe zamijeni hemocijaninom. U ovom slučaju, uobičajeni sadržaj tvari u krvi, a posebice aminokiseline, je poremećen. Također, hemocjanin stvara kompleks s ugljičnim dioksidom tako da "plava krv" ima tendenciju stvaranja krvnih ugrušaka.
 Kako funkcionira biosinteza proteina?
Kako funkcionira biosinteza proteina? Koji su jednostavni organski spojevi proteini? Struktura i svojstva funkcija
Koji su jednostavni organski spojevi proteini? Struktura i svojstva funkcija Fizička svojstva proteina. Najvažnija kemijska svojstva proteina
Fizička svojstva proteina. Najvažnija kemijska svojstva proteina Što je ribosom? Struktura ribosoma
Što je ribosom? Struktura ribosoma Globularni i fibrilarni proteini: osnovne karakteristike
Globularni i fibrilarni proteini: osnovne karakteristike Što je polysom. Struktura polysoma prokariota i eukariota
Što je polysom. Struktura polysoma prokariota i eukariota Proteini: klasifikacija proteina, struktura i funkcije
Proteini: klasifikacija proteina, struktura i funkcije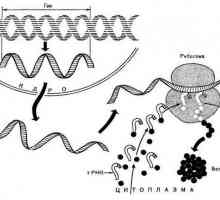 U procesu sinteze proteina, koje strukture i molekule izravno sudjeluju?
U procesu sinteze proteina, koje strukture i molekule izravno sudjeluju? Protein kvartarne strukture: značajke strukture i funkcioniranja
Protein kvartarne strukture: značajke strukture i funkcioniranja Koja je uloga citoplazme u biosintezi proteina? Opis, postupak i funkcije
Koja je uloga citoplazme u biosintezi proteina? Opis, postupak i funkcije Struktura DNA i strukture RNA
Struktura DNA i strukture RNA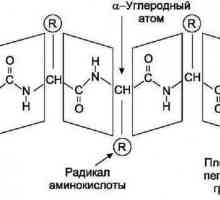 Od aminokiselinskih ostataka molekula onoga što se gradi?
Od aminokiselinskih ostataka molekula onoga što se gradi? Makromolekula je molekula s visokom molekularnom masom. Konfiguracija makromolekule
Makromolekula je molekula s visokom molekularnom masom. Konfiguracija makromolekule Fibrilarni i globularni protein, protein monomer, uzorci sinteze proteina
Fibrilarni i globularni protein, protein monomer, uzorci sinteze proteina Protein: probava u tijelu
Protein: probava u tijelu Razine strukturne organizacije proteinske molekule ili strukture proteina
Razine strukturne organizacije proteinske molekule ili strukture proteina Razine strukturne organizacije proteinske molekule: sekundarna struktura proteina
Razine strukturne organizacije proteinske molekule: sekundarna struktura proteina Kemijski sastav stanice
Kemijski sastav stanice Sinteza proteina
Sinteza proteina Najveće ćelije organske tvari
Najveće ćelije organske tvari Primarna struktura proteina
Primarna struktura proteina
 Koji su jednostavni organski spojevi proteini? Struktura i svojstva funkcija
Koji su jednostavni organski spojevi proteini? Struktura i svojstva funkcija Fizička svojstva proteina. Najvažnija kemijska svojstva proteina
Fizička svojstva proteina. Najvažnija kemijska svojstva proteina Što je ribosom? Struktura ribosoma
Što je ribosom? Struktura ribosoma Globularni i fibrilarni proteini: osnovne karakteristike
Globularni i fibrilarni proteini: osnovne karakteristike Što je polysom. Struktura polysoma prokariota i eukariota
Što je polysom. Struktura polysoma prokariota i eukariota Proteini: klasifikacija proteina, struktura i funkcije
Proteini: klasifikacija proteina, struktura i funkcije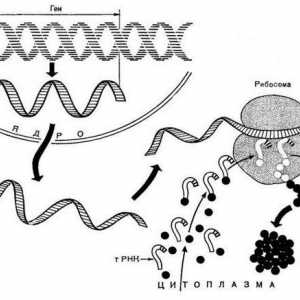 U procesu sinteze proteina, koje strukture i molekule izravno sudjeluju?
U procesu sinteze proteina, koje strukture i molekule izravno sudjeluju? Protein kvartarne strukture: značajke strukture i funkcioniranja
Protein kvartarne strukture: značajke strukture i funkcioniranja Koja je uloga citoplazme u biosintezi proteina? Opis, postupak i funkcije
Koja je uloga citoplazme u biosintezi proteina? Opis, postupak i funkcije